Études relatives au fonctionnement
La littérature scientifique décrit différents effets de l’électrostimulation sur la rétine1-14 : les impulsions électriques stimulent les voies de signal biochimiques qui commandent les processus physiologiques, et dans ce cas au sein des cellules de la rétine. Il se produit des effets neuroprotecteurs et cette protection peut interrompre la progression de la rétinite pigmentaire (RP) et d’autres maladies rétiniennes dégénératives ou au moins les ralentir.
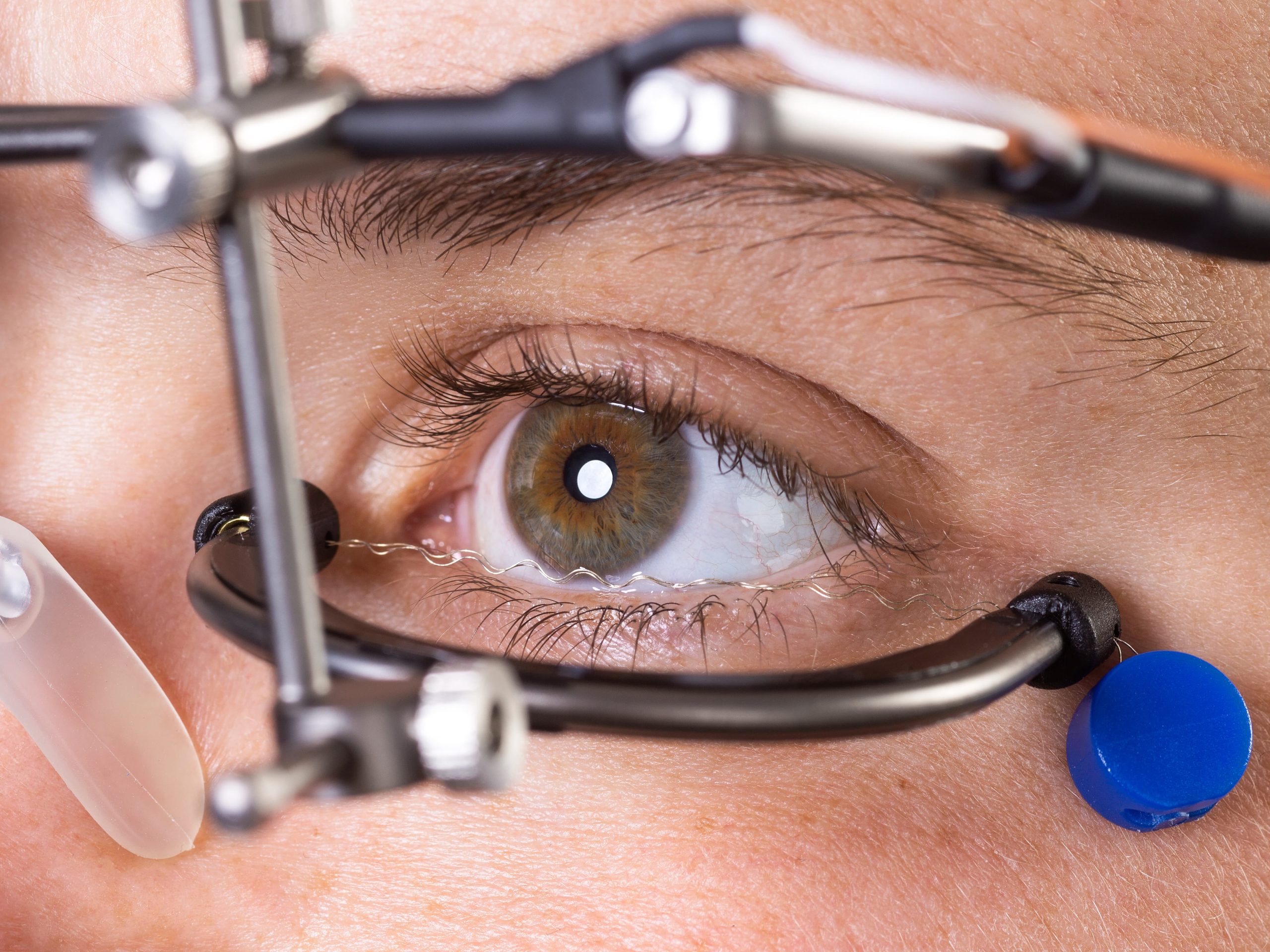
Des études démontrent la sécurité et l’efficacité de la thérapie OkuStim
En 2011, une première étude clinique (EST1) menée auprès de patients atteints de RP a démontré que l’électrostimulation de la rétine est efficace et sûre15. Une étude consécutive (EST2) et une étude observationnelle (TESOLA) ont confirmé les résultats de 2014 à 201616,17.
Une évaluation exploratoire récente des données collectées en 2014 fournit à présent des preuves supplémentaires de l’efficacité de la thérapie OkuStim. Les données montrent qu’après un an de traitement TES, la détérioration du champ visuel des patients atteints de rétinite pigmentaire (RP) était ralentie en fonction de l’intensité de la stimulation21.
Une application sûre
Au total, l’ensemble des patients participants ont suivi le traitement par OkuStim pendant plus de 130 années d’utilisation sans incident de sécurité. La sécurité a été confirmée entre autres par l’étude observationnelle17 précitée.
Par ailleurs, le groupe de travail sur les questions cliniques (Arbeitskreis Klinische Fragen [AKF]) du Conseil médico-scientifique de PRO RETINA Deutschland e. V. estime que l’application du système OkuStim s’avère sûre et n’émet aucune objection à l’application contrôlée auprès de patients atteints d’une rétinite pigmentaire et d’autres graves dystrophies rétiniennes héréditaires généralisées, telles que les dystrophies cônes-bâtonnets, les choroïdérémie ou le syndrome d’Usher.
Une application efficace
Plusieurs études ont démontré les effets de préservation cellulaire de l’électrostimulation qui peuvent ralentir la progression de la maladie (un article récapitulatif figure ici18). L’étude à long terme plus étendue EST216 indique tout particulièrement une diminution de la perte de champ visuel permise par l’électrostimulation. La réaction de la rétine à de brefs éclairs de lumière analysée par électrorétinographie, ou ERG, a permis de constater des effets positifs.
La publication d’une analyse approfondie des données EST2 a permis de décrire pour la première fois le ralentissement dose-dépendant de la perte du champ visuel par le TES21.
Par ailleurs, une étude rétrospective non menée par Okuvision et regroupant près de 100 patients présente un effet positif statistiquement significatif généré par l’électrostimulation sur le champ visuel19. Il est ici intéressant de noter que cet effet positif n’était plus démontrable après 6 mois sans traitement. Cela indique que le traitement par le système OkuStim doit être exécuté le plus longtemps possible et sans interruption prolongée.
Recommandation d'action
Depuis 2021, la stimulation électrique transcornéenne est mentionnée dans les directives ophtalmologiques pour les maladies héréditaires de la rétine, de la choroïde et des voies visuelles comme option thérapeutique pour la rétinite pigmentaire (RP). Cela donne aux ophtalmologues une option d’action concrète pour le traitement symptomatique de la RP et donc la possibilité de retarder des handicaps graves dans la vie quotidienne dus à la perte de la vue.
Études actuelles
Étude observationnelle
Au cours de l’été 2021, une deuxième étude d’observation à grande échelle a été lancée auprès de patients utilisant le système OkuStim. Tous les utilisateurs d’OkuStim qui stimulent depuis au moins un an ou qui ont stimulé pendant au moins un an pouvaient participer.
La collecte des données sur les bénéfices objectifs et subjectifs à long terme de la thérapie OkuStim est maintenant terminée et en cours d’analyse. Les résultats sont attendus pour l’année prochaine.
Ces données viendront compléter les résultats précédents sur l’efficacité. Elles devraient aider les scientifiques et les médecins, ainsi que nous, en tant que développeurs et fabricants du système OkuStim, à améliorer encore l’électrostimulation pour vous, les patients.
Étude clinique en cours
Pour que l’électrostimulation rétinienne soit incluse dans le catalogue des prestations des caisses d’assurance maladie légales en Allemagne, davantage de données sur l’efficacité de cette technique sont recueillies auprès des patients sur une période plus longue. L’évaluation des avantages est l’objectif de l’étude expérimentale qui a été lancée sous la direction de l’hôpital ophtalmologique universitaire de Tübingen20. Le coût total du traitement sera couvert par les caisses d’assurance maladie allemandes pendant toute la durée de l’essai.
Le recrutement pour cette étude est terminé. Les premiers résultats sont attendus pour 2026.
Nous avons éveillé votre intérêt pour plus de détails sur les études et l’effet du traitement avec le système OkuStim ? Vous trouverez plus d’informations ici :
Vous trouverez des liens vers les différentes études dans les références ci-dessous
Références:
- Morimoto T, Miyoshi T, Matsuda S, Tano Y, Fujikado T, Fukuda Y. Transcorneal electrical stimulation rescues axotomized retinal ganglion cells by activating endogenous retinal IGF-1 system. Invest Ophthalmol Vis Sci. 2005 Jun;46(6):2147-55.
- Geremia NM, Gordon T, Brushart TM, Al-Majed AA, Verge VM. Electrical stimulation promotes sensory neuron regeneration and growth-associated gene expression. Exp Neurol. 2007 Jun;205(2):347-59.
- Sato T, Fujikado T, Lee TS, Tano Y. Direct effect of electrical stimulation on induction of brain-derived neurotrophic factor from cultured retinal Müller cells. Invest Ophthalmol Vis Sci. 2008 Oct;49(10):4641-6.
- Schmid H, Herrmann T, Kohler K, Stett A. Neuroprotective effect of transretinal electrical stimulation on neurons in the inner nuclear layer of the degenerated retina. Brain Res Bull. 2009 Apr 6;79(1):15-25.
- Ciavatta VT, Kim M, Wong P, Nickerson JM, Shuler RK Jr, McLean GY, Pardue MT. Retinal expression of Fgf2 in RCS rats with subretinal microphotodiode array. Invest Ophthalmol Vis Sci. 2009 Oct;50(10):4523-30.
- Ni YQ, Gan DK, Xu HD, Xu GZ, Da CD. Neuroprotective effect of transcorneal electrical stimulation on light-induced photoreceptor degeneration. Exp Neurol. 2009 Oct;219(2):439-52.
- Morimoto T, Kanda H, Kondo M, Terasaki H, Nishida K, Fujikado T. Transcorneal electrical stimulation promotes survival of photoreceptors and improves retinal function in rhodopsin P347L transgenic rabbits. Invest Ophthalmol Vis Sci. 2012 Jun 28;53(7):4254-61.
- Zhou WT, Ni YQ, Jin ZB, Zhang M, Wu JH, Zhu Y, Xu GZ, Gan DK. Electrical stimulation ameliorates light-induced photoreceptor degeneration in vitro via suppressing the proinflammatory effect of microglia and enhancing the neurotrophic potential of Müller cells. Exp Neurol. 2012 Dec;238(2):192-208.
- Osako T, Chuman H, Maekubo T, Ishiai M, Kawano N, Nao-I N. Effects of steroid administration and transcorneal electrical stimulation on the anatomic and electrophysiologic deterioration of nonarteritic ischemic optic neuropathy in a rodent model. Jpn J Ophthalmol. 2013 Jul;57(4):410-5.
- Ozeki N, Shinoda K, Ohde H, Ishida S, Tsubota K. Improvement of visual acuity after transcorneal electrical stimulation in case of Best vitelliform macular dystrophy. Graefes Arch Clin Exp Ophthalmol. 2013 Jul;251(7):1867-70.
- Fu L, Lo AC, Lai JS, Shih KC. The role of electrical stimulation therapy in ophthalmic diseases. Graefes Arch Clin Exp Ophthalmol. 2015 Feb;253(2):171-6.
- Kanamoto T, Souchelnytskyi N, Kurimoto T, Ikeda Y, Sakaue H, Munemasa Y, Kiuchi Y. Proteomic study of retinal proteins associated with transcorneal electric stimulation in rats. J Ophthalmol. 2015;2015:492050.
- Hanif AM, Kim MK, Thomas JG, Ciavatta VT, Chrenek M, Hetling JR, Pardue MT. Whole-eye electrical stimulation therapy preserves visual function and structure in P23H-1 rats. Exp Eye Res. 2016 Aug;149:75-83.
- Della Volpe-Waizel M, Zuche HC, Müller U, Rickmann A, Scholl HPN, Todorova MG. Metabolic monitoring of transcorneal electrical stimulation in retinitis pigmentosa. Graefes Arch Clin Exp Ophthalmol. 2020 Jan;258(1):79-87. LINK
- Schatz A, Röck T, Naycheva L, Willmann G, Wilhelm B, Peters T, Bartz-Schmidt KU, Zrenner E, Messias A, Gekeler F. Transcorneal electrical stimulation for patients with retinitis pigmentosa: a prospective, randomized, sham-controlled exploratory study. Invest Ophthalmol Vis Sci. 2011 Jun 23;52(7):4485-96. LINK
- Schatz A, Pach J, Gosheva M, Naycheva L, Willmann G, Wilhelm B, Peters T, Bartz-Schmidt KU, Zrenner E, Messias A, Gekeler F. Transcorneal Electrical Stimulation for Patients With Retinitis Pigmentosa: A Prospective, Randomized, Sham-Controlled Follow-up Study Over 1 Year. Invest Ophthalmol Vis Sci. 2017 Jan 1;58(1):257-269. LINK
- Jolly JK, Wagner SK, Martus P, MacLaren RE, Wilhelm B, Webster AR, Downes SM, Charbel Issa P, Kellner U, Jägle H, Rüther K, Bertelsen M, Bragadóttir R, Prener Holtan J, van den Born LI, Sodi A, Virgili G, Gosheva M, Pach J, Zündorf I, Zrenner E, Gekeler F. Transcorneal Electrical Stimulation for the Treatment of Retinitis Pigmentosa: A Multicenter Safety Study of the OkuStim® System (TESOLA-Study). Ophthalmic Res. 2020;63(3):234-243. LINK
- Liu J, Tong K, Lin Y, Lee VWH, So KF, Shih KC, Lai JSM, Chiu K. Effectiveness of Microcurrent Stimulation in Preserving Retinal Function of Blind Leading Retinal Degeneration and Optic Neuropathy: A Systematic Review. Neuromodulation. 2021 May 13. doi: 10.1111/ner.13414. Epub ahead of print. PMID: 33984873.
- Sinim Kahraman N, Oner A. Effect of Transcorneal Electrical Stimulation on Patients with Retinitis Pigmentosa. J Ocul Pharmacol Ther. 2020 Oct;36(8):609-617. LINK
- Kahle N, Peters T, Braun A, Franklin J, Michalik C, Gekeler F, Wilhelm B; retina.net e. V.; TES-RP-Studiengruppe. Transkorneale Elektrostimulation bei Retinitis pigmentosa : Prüfplan einer multizentrischen, prospektiven, randomisierten, kontrollierten und doppelblinden Studie im Auftrag des Gemeinsamen Bundesausschusses (G-BA-Erprobungsrichtlinie) [Transcorneal electrostimulation in retinitis pigmentosa : Protocol of a multicentric prospective, randomized, controlled and double-masked trial on behalf of the Joint Federal Committee (G-BA pilot regulation)]. 2021 May;118(5):512-516. LINK
- Stett A, Schatz A, Gekeler F, Franklin J. Transcorneal Electrical Stimulation Dose-Dependently Slows the Visual Field Loss in Retinitis Pigmentosa. Transl Vis Sci Technol. 2023;12(2):29. doi:10.1167/tvst.12.2.29 LINK