Klinische Studien
Hier finden Sie Informationen und Links zum wissenschaftlichen Hintergrund der Elektrostimulation der Netzhaut und der OkuStim-Therapie. Gerne können Sie uns direkt ansprechen, wenn Sie noch weitere Informationen wünschen oder noch Fragen haben.
Studienlage zur Wirkungsweise
In der wissenschaftlichen Literatur sind verschiedene Effekte der Elektrostimulation auf die Netzhaut beschrieben1-14: Elektrische Impulse stoßen biochemische Signalwege an, die physiologische Vorgänge steuern – in diesem Fall in den Zellen der Netzhaut. Es kommt zu neuroprotektiven Effekten und diese Schutzwirkung kann ein Fortschreiten von Retinitis pigmentosa (RP) und anderen degenerativen Netzhaut-Erkrankungen aufhalten oder zumindest verlangsamen.
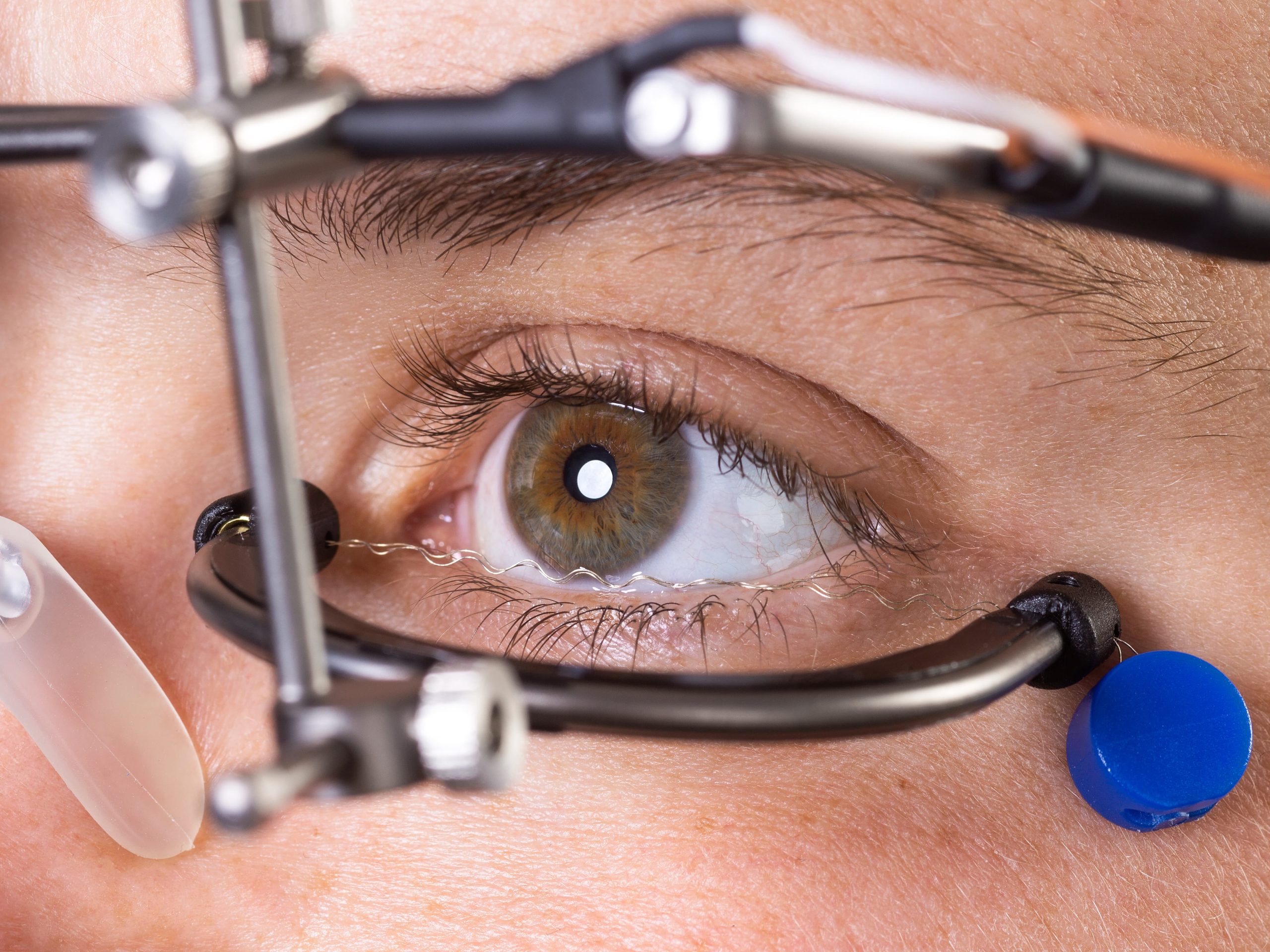
Studien belegen Sicherheit und Wirksamkeit der OkuStim-Therapie
2011 zeigte eine erste klinische Studie (EST1) mit RP-Patienten, dass die Elektrostimulation der Netzhaut wirksam und sicher ist15. Eine Folgestudie (EST2) und eine Anwendungsbeobachtung (TESOLA) bestätigten 2014/2016 die Ergebnisse16,17. Eine aktuelle explorative Auswertung der 2014 erhobenen Daten liefert nun weitere Belege für die Wirksamkeit der OkuStim-Therapie. Die Daten zeigen, dass nach einem Jahr TES-Behandlung die Gesichtsfeldverschlechterung bei Patienten mit Retinitis pigmentosa (RP) in Abhängigkeit von der Stimulationsstärke verlangsamt war21.
Sichere Anwendung
Alle Studienpatienten zusammengenommen hat die OkuStim-Behandlung bereits über 130 Anwendungsjahre ohne sicherheitsrelevante Zwischenfälle hinter sich. Die Sicherheit wurde unter anderem durch die oben genannte Anwendungsbeobachtung17 bestätigt.
Zudem bewertet der Arbeitskreis Klinische Fragen (AKF) des Wissenschaftlich-Medizinischen Beirats von PRO RETINA Deutschland e. V. die Anwendung des OkuStim-Systems als sicher und hat keine Einwände gegen die kontrollierte Anwendung bei Patienten mit Retinitis pigmentosa und anderen generalisierten erblichen Netzhautdystrophien wie Zapfen-und-Stäbchen-Dystrophien, Choroideremie oder Usher-Syndrom.
Wirksame Anwendung
Mehrere Studien zeigten die zellerhaltenden Effekte der Elektrostimulation, die ein Fortschreiten der Erkrankung bremsen können (einen zusammenfassenden Artikel finden Sie hier18). Besonders die größere Langzeitsstudie EST216 deutet auf eine Verminderung des Gesichtsfeldverlusts durch Elektrostimulation hin. Auch die Reaktion der Netzhaut auf kurze Lichtblitze, die mit Elektroretinographie, kurz ERG, untersucht wurde, zeigte positive Effekte.
Mit der Veröffentlichung einer erweiterten Auswertung der EST2-Daten wird nun erstmals die dosisabhängige Verlangsamung des Gesichtsfeldverlustes durch TES beschrieben21.
Außerdem weist eine rückblickende, nicht von Okuvision durchgeführte Studie mit rund 100 Patienten einen statistisch signifikanten positiven Einfluss der Elektrostimulation auf das Gesichtsfeld nach19. Das Interessante hier ist, dass dieser positive Einfluss nach 6 Monaten ohne Behandlung nicht mehr nachweisbar war. Das legt nahe, die Behandlung mit dem OkuStim-System möglichst dauerhaft und ohne lange Unterbrechungen anzuwenden.
Handlungsempfehlung
Seit 2021 wird die transkorneale Elektrostimulation in der augenärztlichen Leitlinie für Erbliche Netzhaut-, Aderhaut- und Sehbahnerkrankungen als Option zur Therapie bei Retinitis Pigmentosa (RP) genannt. Dies gibt Augenärzten eine konkrete Handlungsoption zur symptomatischen Behandlung von RP und damit die Möglichkeit, schwere Beeinträchtigungen im Alltag durch Sehkraftverlust hinauszuzögern.
Aktuelle Studien
Anwendungsbeobachtung
Im Sommer 2021 begann eine zweite Anwendungsbeobachtung mit Patienten, die das OkuStim-System nutzen. Daran konnten alle OkuStim-Anwender, die seit mindestens einem Jahr stimulieren oder mindestens ein Jahr lang stimuliert haben, teilnehmen.
Die Datenerhebung zum objektiven und subjektiven Langzeit-Nutzen der OkuStim-Therapie ist jetzt abgeschlossen und die Auswertung läuft. Mit Ergebnissen ist kommendes Jahr zu rechnen.
Die Daten sollen die bisherigen Ergebnisse zur Wirksamkeit ergänzen. Sie sollen den Wissenschaftlern und Ärzten sowie uns als Entwicklern und Produzenten des OkuStim-Systems helfen, die Elektrostimulation für Sie die Patienten weiter zu verbessern.
Laufende Klinische Studie – Erprobungsstudie TES-RP
Damit die Elektrostimulation der Netzhaut in den Leistungskatalog der gesetzlichen Krankenkassen in Deutschland aufgenommen werden kann, werden noch mehr Patientendaten zur Wirksamkeit über einen längeren Zeitraum gesammelt. Die Nutzenbewertung ist Ziel der Erprobungsstudie, die unter Leitung der Universitäts-Augenklinik Tübingen gestartet wurde20. Die gesamten Behandlungskosten werden für den Zeitraum der Studie von den deutschen gesetzlichen Krankenkassen übernommen.
Die Rekrutierung für diese Studie ist nun abgeschlossen. Mit ersten Ergebnissen wird 2026 gerechnet.
Haben wir Ihr Interesse geweckt an weiteren Details zu den Studien und der Wirkung einer Behandlung mit dem OkuStim-System? Dann finden Sie hier weitere Informationen:
Links zu den einzelnen Studien finden Sie unten in den Referenzen
Referenzen:
- Morimoto T, Miyoshi T, Matsuda S, Tano Y, Fujikado T, Fukuda Y. Transcorneal electrical stimulation rescues axotomized retinal ganglion cells by activating endogenous retinal IGF-1 system. Invest Ophthalmol Vis Sci. 2005 Jun;46(6):2147-55.
- Geremia NM, Gordon T, Brushart TM, Al-Majed AA, Verge VM. Electrical stimulation promotes sensory neuron regeneration and growth-associated gene expression. Exp Neurol. 2007 Jun;205(2):347-59.
- Sato T, Fujikado T, Lee TS, Tano Y. Direct effect of electrical stimulation on induction of brain-derived neurotrophic factor from cultured retinal Müller cells. Invest Ophthalmol Vis Sci. 2008 Oct;49(10):4641-6.
- Schmid H, Herrmann T, Kohler K, Stett A. Neuroprotective effect of transretinal electrical stimulation on neurons in the inner nuclear layer of the degenerated retina. Brain Res Bull. 2009 Apr 6;79(1):15-25.
- Ciavatta VT, Kim M, Wong P, Nickerson JM, Shuler RK Jr, McLean GY, Pardue MT. Retinal expression of Fgf2 in RCS rats with subretinal microphotodiode array. Invest Ophthalmol Vis Sci. 2009 Oct;50(10):4523-30.
- Ni YQ, Gan DK, Xu HD, Xu GZ, Da CD. Neuroprotective effect of transcorneal electrical stimulation on light-induced photoreceptor degeneration. Exp Neurol. 2009 Oct;219(2):439-52.
- Morimoto T, Kanda H, Kondo M, Terasaki H, Nishida K, Fujikado T. Transcorneal electrical stimulation promotes survival of photoreceptors and improves retinal function in rhodopsin P347L transgenic rabbits. Invest Ophthalmol Vis Sci. 2012 Jun 28;53(7):4254-61.
- Zhou WT, Ni YQ, Jin ZB, Zhang M, Wu JH, Zhu Y, Xu GZ, Gan DK. Electrical stimulation ameliorates light-induced photoreceptor degeneration in vitro via suppressing the proinflammatory effect of microglia and enhancing the neurotrophic potential of Müller cells. Exp Neurol. 2012 Dec;238(2):192-208.
- Osako T, Chuman H, Maekubo T, Ishiai M, Kawano N, Nao-I N. Effects of steroid administration and transcorneal electrical stimulation on the anatomic and electrophysiologic deterioration of nonarteritic ischemic optic neuropathy in a rodent model. Jpn J Ophthalmol. 2013 Jul;57(4):410-5.
- Ozeki N, Shinoda K, Ohde H, Ishida S, Tsubota K. Improvement of visual acuity after transcorneal electrical stimulation in case of Best vitelliform macular dystrophy. Graefes Arch Clin Exp Ophthalmol. 2013 Jul;251(7):1867-70.
- Fu L, Lo AC, Lai JS, Shih KC. The role of electrical stimulation therapy in ophthalmic diseases. Graefes Arch Clin Exp Ophthalmol. 2015 Feb;253(2):171-6.
- Kanamoto T, Souchelnytskyi N, Kurimoto T, Ikeda Y, Sakaue H, Munemasa Y, Kiuchi Y. Proteomic study of retinal proteins associated with transcorneal electric stimulation in rats. J Ophthalmol. 2015;2015:492050.
- Hanif AM, Kim MK, Thomas JG, Ciavatta VT, Chrenek M, Hetling JR, Pardue MT. Whole-eye electrical stimulation therapy preserves visual function and structure in P23H-1 rats. Exp Eye Res. 2016 Aug;149:75-83.
- Della Volpe-Waizel M, Zuche HC, Müller U, Rickmann A, Scholl HPN, Todorova MG. Metabolic monitoring of transcorneal electrical stimulation in retinitis pigmentosa. Graefes Arch Clin Exp Ophthalmol. 2020 Jan;258(1):79-87. LINK
- Schatz A, Röck T, Naycheva L, Willmann G, Wilhelm B, Peters T, Bartz-Schmidt KU, Zrenner E, Messias A, Gekeler F. Transcorneal electrical stimulation for patients with retinitis pigmentosa: a prospective, randomized, sham-controlled exploratory study. Invest Ophthalmol Vis Sci. 2011 Jun 23;52(7):4485-96. LINK
- Schatz A, Pach J, Gosheva M, Naycheva L, Willmann G, Wilhelm B, Peters T, Bartz-Schmidt KU, Zrenner E, Messias A, Gekeler F. Transcorneal Electrical Stimulation for Patients With Retinitis Pigmentosa: A Prospective, Randomized, Sham-Controlled Follow-up Study Over 1 Year. Invest Ophthalmol Vis Sci. 2017 Jan 1;58(1):257-269. LINK
- Jolly JK, Wagner SK, Martus P, MacLaren RE, Wilhelm B, Webster AR, Downes SM, Charbel Issa P, Kellner U, Jägle H, Rüther K, Bertelsen M, Bragadóttir R, Prener Holtan J, van den Born LI, Sodi A, Virgili G, Gosheva M, Pach J, Zündorf I, Zrenner E, Gekeler F. Transcorneal Electrical Stimulation for the Treatment of Retinitis Pigmentosa: A Multicenter Safety Study of the OkuStim® System (TESOLA-Study). Ophthalmic Res. 2020;63(3):234-243. LINK
- Liu J, Tong K, Lin Y, Lee VWH, So KF, Shih KC, Lai JSM, Chiu K. Effectiveness of Microcurrent Stimulation in Preserving Retinal Function of Blind Leading Retinal Degeneration and Optic Neuropathy: A Systematic Review. Neuromodulation. 2021 May 13. doi: 10.1111/ner.13414. Epub ahead of print. PMID: 33984873.
- Sinim Kahraman N, Oner A. Effect of Transcorneal Electrical Stimulation on Patients with Retinitis Pigmentosa. J Ocul Pharmacol Ther. 2020 Oct;36(8):609-617. LINK
- Kahle N, Peters T, Braun A, Franklin J, Michalik C, Gekeler F, Wilhelm B; retina.net e. V.; TES-RP-Studiengruppe. Transkorneale Elektrostimulation bei Retinitis pigmentosa : Prüfplan einer multizentrischen, prospektiven, randomisierten, kontrollierten und doppelblinden Studie im Auftrag des Gemeinsamen Bundesausschusses (G-BA-Erprobungsrichtlinie) [Transcorneal electrostimulation in retinitis pigmentosa : Protocol of a multicentric prospective, randomized, controlled and double-masked trial on behalf of the Joint Federal Committee (G-BA pilot regulation)]. 2021 May;118(5):512-516. LINK
- Stett A, Schatz A, Gekeler F, Franklin J. Transcorneal Electrical Stimulation Dose-Dependently Slows the Visual Field Loss in Retinitis Pigmentosa. LINK